单级好氧和限氧污水处理系统中总氮损失的微生物学机理*
张 悦1 曾 薇1** 刘春兰2 李 磊1 杨莹莹1 彭永臻1
(1北京工业大学环境与能源工程学院 北京 100124; 2杭州市财政性投资项目评审中心 杭州 310009)
摘 要 :近年来,单级好氧和限氧污水处理系统中总氮损失的现象引起了人们的普遍关注,本文对这种现象的微生物学机理及研究现状进行了阐述,主要是几类细菌的单独脱氮或者它们之间的协同脱氮,包括自养(亚) 硝化菌单独脱氮、好氧反硝化菌单独脱氮、(亚)硝化菌和好氧反硝化菌的协同脱氮以及(亚)硝化菌和厌氧氨氧化菌的协同脱氮. 与传统的硝化-反硝化脱氮工艺相比,这些脱氮新途径具有不可比拟的优越性,对于强化污水生物脱氮具有重要意义. 图8 参53
关键词 :总氮损失;好氧反硝化;厌氧氨氧化;限氧
CLC X703
Microbiological Mechanism of Nitrogen Loss in Aerobic or Oxygen-limited Wastewater Treatment System*
(1College of Environmental and Energy Engineering, Beijing University of Technology, Beijing 100124, China) (2Evaluation Center of Hangzhou Government Investing Project, Hangzhou 310009, China)
Abstract In recent years, the phenomenon of total nitrogen loss which is found in single aerobic or oxygen-limited wastewater treatment systems has attracted researchers’ concern. Microbiological theory and related studies of nitrogen loss were reviewed in this paper. It involves the different groups of bacteria alone or in cooperation, including nitrogen removal by autotrophic nitrifying bacteria and aerobic denitrifying bacteria, the inter-synthesis between nitrifying bacteria and aerobic denitrifying bacteria; and the cooperation of nitrifying bacteria and anaerobic ammonia oxidation (Anammox) bacteria. The new biological nitrogen removal mechanisms, which have incomparable advantages to the traditional nitrification-denitrification nitrogen removal technique, have important significance to enhance nitrogen removal in wastewater treatment. Fig 8, Ref 53
Keywords nitrogen loss; aerobic denitrification; anaerobic ammonia oxidation (Anammox); oxygen-limited
CLC X703
传统生物脱氮理论认为生物脱氮包括硝化和反硝化两个阶段,相应的功能微生物分别是硝化细菌和反硝化细菌. 硝化细菌通常是自养型好氧微生物,主要由亚硝化菌和硝化菌两类构成,分别从NH3-N和NO2-N的氧化过程中获得能量,需要O2 作为呼吸的最终电子受体;反硝化细菌大都是异养型兼性厌氧菌,在厌氧条件下从有机物的氧化过程中获取能量,将NO3-N (或NO2-N)作为无氧呼吸时的电子受体. 由于硝化细菌和反硝化细菌各自适宜的生长条件不同,现行的生物脱氮工艺几乎都是将硝化和反硝化过程独立运行[1],如代表性的Bardenpho、A/O、A2O、UCT、双沟式氧化沟工艺(从空间上分开)和SBR工艺(从时间上分开). 但是,近十余年来,在很多单级好氧或限氧的污水处理系统中都发现了总氮损失现象[2~5],总氮损失率高达30%~51%,这一现象有悖于传统脱氮理论,其微生物学机理已成为研究热点。
所谓“单级污水处理系统中的总氮损失”,就是通过脱氮微生物的协同作用,在同一空间、同一时间内完成氨氮(NH3-N)等化合态氮向氮气或气态氮氧化物转化的过程,由此,不仅氨氮得到去除,而且水处理系统中总氮浓度明显降低. 目前,从物理学角度以“微环境理论”解释这种现象已被普遍接受. 该理论认为,在单级系统中由于活性污泥絮体或者生物膜中的氧的浓度梯度使得硝化和反硝化同时进行. 近年来,关于脱氮微生物种类和代谢途径多样性的研究有了很大进展,发现了几种新的脱氮途径和功能微生物,这不仅为单级系统中总氮损失现象提供了更加合理的解释,而且也为进一步探索新的生物脱氮技术奠定了理论基础. 本文在传统脱氮理论的基础上,结合当前国内外研究现状,对引起单级污水处理系统中总氮损失的功能微生物及其微生物学机制进行阐述。
1 自养(亚)硝化菌脱氮
化作用下将NH3-N转化为NH2OH,然后在羟氨氧化酶(HAO)的催化作用下将NH2OH氧化为NO2-N (式①、②);硝化菌在亚硝酸氧化酶(NOR)的催化作用下将NO2-N氧化为NO3-N(式③).
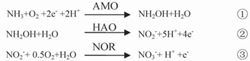
上述传统脱氮理论在自然界氮物质循环中发挥着重要的作用. 传统理论认为,无论是亚硝化菌还是硝化菌都不能单独将NH3-N转化为N2或气态氮氧化物. 但随着研究的不断深入,发现了某些(亚)硝化菌具有不同于传统脱氮理论的其
他脱氮途径,从而为污水生物脱氮的强化开辟了新途径.
1.1 自养(亚)硝化菌的反硝化脱氮
研究表明,某些亚硝化菌和硝化菌具有部分或者全部的反硝化功能. 在相关研究中对亚硝化菌具有反硝化功能的报道相对多一些,但不排除某些硝化菌也具有反硝化功能. 早在1972年就有研究报道,在微藻类条件下某些自养硝化菌可以在好氧或厌氧条件下还原亚硝酸盐产生N O [6]. Bock等分别在1988和1995年先后证实了硝化细菌中的亚硝化单胞菌属(Nitrosomonas)和硝化杆菌属(Nitrobacter)在厌氧条件下具有反硝化能力[7, 8]. 近年有研究表明Nitrosomonas菌属中的N. europaea [9]和N. eutropha [10]具有反硝化能力,能够在低氧量的状态下氧化NH -N产生N O、NO或N . Wrage等的研究同样表明,NH -N被氧化为NO -N后可以被自养亚硝化菌的还原酶系还原生成N O和N ,整个过程由自养菌完成[11].
Wrage [11]、Shrestha [12]等先后对亚硝化菌的硝化–反硝化脱氮的代谢途径进行研究,认为亚硝化菌的硝化–反硝化过程是在一系列氧化酶系(硝化过程)和还原酶系(反硝化过程)的催化作用下分别进行的,这和传统硝化–反硝化理论相似,不同的是整个过程由亚硝化菌单独完成. 其总结的代谢途径如图1所示.
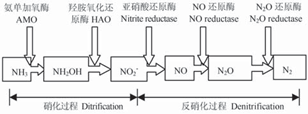
图1 亚硝化菌的硝化–反硝化代谢途径[11, 12]
Fig. 1 Nitrification and denitrification carried out by ammonia-oxidizing bacteria [11, 12]
与上述理论不同,有研究者将自养(亚)硝化菌的单独脱氮归结为硝化–反硝化的耦合作用(图2) [10, 14],即认为硝化过程和反硝化过程相互依赖于微生物体内的NADH呼吸链. Naqvi采用氮的同位素示踪法研究阿拉伯海域内N2O的产生机理,观察到当硝化反应和反硝化反应分别发生时没有产生被标记的N2O,因此得出同样结论,即N2O很有可能是由某些硝化菌的硝化–反硝化耦合作用产生的[13].
相对于传统反硝化来说,自养(亚)硝化菌的反硝化效率非常低. Ralf等的试验证明,在高氨溶液[氨氮浓度700 mg (N)L-1]中单独培养的Nitrosomonas将NH -N转化为NO -N后,仅能将0.28%的NO -N还原[15];Tallec的研究表明,当DO浓度为 0.4~1.1 mg (O2)/L时,由某些硝化菌反硝化产生的N2O占总N2O 产量的60%,N O总量占NO -N损失的0.4% [16];Wrage认为由硝化菌反硝化产生的N O仅占总N O产量的30% [11]. 另有研究者对亚硝化系统的研究结果表明,自养亚硝酸菌能将总氮的0.2%转化为NO,1.7%转化为N O [17].
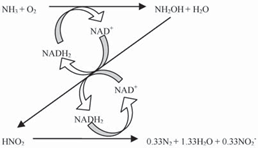
2 自养硝化菌脱氮的假设途径[10, 14]
Fig. 2 Hypothetical model of autotrophic nitrifying bacteria [10, 14]
Schmidt等对硝化过程中释放NO等氮氧化物的现象进行了大量研究,揭示此现象是基于亚硝化菌中Nitrosomonas 类细菌的作用,提出缺氧条件下的NO 循环模型(图3) [18]. NO 和NO2 之间不断循环转化,在缺氧条件下活性更强的NO2代替O2作为电子受体,从而实现AMO对NH3-N的氧化过程.
现在已经确认的是N. eutropha、N. europaea和Nitrosolobusmultiformis都能进行上述反应途径. Schmidt等将其反应方程式归纳为:
NH +N O +H++2e- → NH OH+2NO+H O
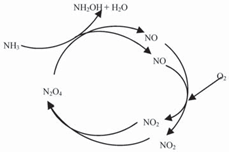
图3 NO 循环作用下Nitrosomonas类细菌的缺氧氨氧化假设模型[18]
Fig. 3 Hypothetical model of anoxic ammonia oxidation by Nitrosomonas-like bacteria [18]
对于反应式中N2O4 (NO2)的来源,有研究者认为,在限氧条件下,硝化单胞菌可在菌体内先形成NO,NO被溶解氧氧化为N2O4,然后在缺氧环境下NH3-N被N2O4氧化,终产物为NO、N O、N [19]. 也有研究者直接向反应系统内通入痕量的NO2 (N2O4)气体来促进氨氮的去除. 李小鹏通过实验也证明,在无分子氧情况下,亚硝化菌能发生基于NO2的氨氧化, 并且低浓度NO2 (体积分数<5×10 )条件下氨氧化速率较高, 总氮损失也较大[20].
2 好氧反硝化菌脱氮
多菌属如产碱菌属(Alcaligenes) [22]、克雷伯氏菌属(Klebsiella) [23] 和假单胞菌属(Pseudomonas) [24]都具有好氧反硝化功能. 好氧反硝化菌可以和硝化菌协同脱氮,某些好氧反硝化菌同时也是异养硝化菌,可以单独脱氮.
2.1 好氧硝化菌和好氧反硝化菌的协同脱氮
好氧硝化菌和好氧反硝化菌的协同脱氮原理是:NH3-N首先由好氧硝化菌转化为NO3-N (或NO2-N),然后好氧反硝化菌对NO3-N (或NO2-N)进行还原;其公认的还原途径是: NO3-N分别由硝酸还原酶、亚硝酸还原酶、一氧化氮还原酶和一氧化二氮还原酶催化还原为N2.
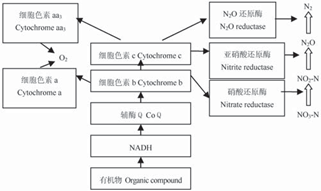
图4 好氧反硝化菌反硝化过程的电子传递模型[26, 27]
Fig. 4 Schematic of branched respiratory electron transport chain of aerobic denitrifying bacteria [25, 26]
早期理论认为,O2 的存在对反硝化过程有抑制作用, 主要表现在O2 相对NO3-N (或NO2-N)优先得电子,而且O2会氧化硝酸还原酶系使其失去催化活性. 后来Korner的研究表明,硝酸还原酶、亚硝酸还原酶和一氧化二氮还原酶对溶解氧的较大耐受浓度分别达到5.1、2.5和3.8 mg/L,说明在限氧条件下细菌的反硝化酶系依然有活性[25]. 目前关于好氧反硝化菌如何同时利用NO - (或NO -)和O 进行呼吸作用的微生物学代谢机制尚未得到一致的结论. 有研究者提出协同呼吸是好氧反硝化的作用机理,协同呼吸意味着氧和硝酸盐同时作为电子受体,有机物提供的电子流同时传输给反硝化酶系统和氧,因此反硝化可以在好氧情况下发生[26, 27]. 这种好氧反硝化菌协同呼吸的电子传递途径如图4所示.
2.2 好氧反硝化细菌的单独脱氮
好氧反硝化细菌的单独脱氮是指某些好氧反硝化细菌同时也是异养硝化菌,其在好氧条件下可单独作用将底物氨氮转化为N2. 目前已报道兼具异养硝化功能的好氧反硝化菌有Pseudomonas stutzeri、Alcaligenes faecalis [28]、Comamonas sp. [29] 、 Thiosphaera pantotropha(Paracoccus denitrifications) [30]等. 研究者较早发现的既可以在好氧条件又可以在缺氧条件下生长的异养反硝化菌是T. pantotropha,并发现它有硝酸盐还原酶,这种酶在有氧的情况下具有活性[31]. Wehrfritz等总结了T. pantotropha将异养硝化和好氧反硝化相结合的代谢模式(图5) [32]:NH -N经T. pantotropha的AMO催化作用转化为NH2OH,然后在HAO催化作用下将NH2OH氧化为NO2-N,利用氧化过程中产生的细胞色素c551作为反硝化酶系的电子供体,将NO2-N还原为含氮气化物. 该研究还进一步说明从T.pantotropha中分离纯化得到的HAO和N. europaea的HAO有显著不同,且二者在羟氨氧化过程中的电子受体和电子传递途径也是不同的.
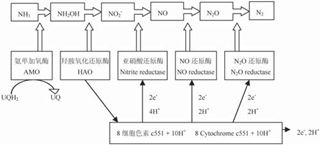
图5 好氧反硝化细菌的单独脱氮电子传递模式[32]
Fig. 5 Hypothetical model of ammonia removal by aerobic denitrifying bacterial [32]
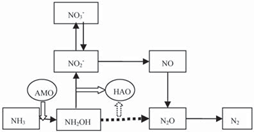
图6 推测的好氧反硝化细菌的脱氮途径[33]
Fig. 6 Hypothetical model of ammonia removal by aerobic denitrifying bacteria [33]
另有研究者推测的好氧反硝化菌可能存在的脱氮途径[33]如图6所示. 图5和图6的关键不同之处在于,图6相对于图5 多了一条氮的转化途径(如图6虚线部分),即NH2OH可以在HAO的催化作用下不经过亚硝酸盐而转化为N2O,进而还原为N2. Rorberson很早(1988年)就证实了此结论,其研究表明在周围环境有溶解氧的情况下,即使没有中间产物亚硝酸盐,T. pantotropha也能够把氨转换为氮气. 较近Joo等研究了
Alcaligenes faecalis No.4的好氧硝化和好氧反硝化能力,发现硝化过程的主要产物是NH2OH,仅有很少的NH3-N转化为 NO -N,因此推测其反硝化过程是通过NH OH完成的[34]. 何霞等对异养硝化细菌Bacillus sp. LY的研究也表明,其脱氮途径很有可能如图6虚线部分所示,并指出可能有一部分硝酸盐或亚硝酸盐生成羟胺,然后通过NH2OH→N2O→N2的方式脱氮[35].
Hippen等在1997年报道了一种适用于处理高浓度含氮废水的新工艺[36]. 在该工艺中,氨转化为氮气的过程不需要按化学计量式消耗电子供体,这种特殊的转化过程命名为“Aerobic deammonification”(好氧反氨化)工艺. 随后又有研究者观察到限氧条件下的总氮损失现象,后用荧光原位杂交技术(FISH)等分子生物学方法证明此现象是自养硝化菌和厌氧氨氧化菌协同脱氮的结果[37~39]. 较近有研究者用生物过滤器处理饮用水,在比正常需氧量低30%的条件下,硝化过程损失了1/3的NH -N,推测这同样是基于上述脱氮机理[40].
自养亚硝化菌和厌氧氨氧化菌的脱氮机理如式④、⑤所示[41],在限氧条件下,NH -N被好氧亚硝化菌氧化成NO -N,消耗氧气创造出缺氧环境(④式),随后厌氧氨氧化菌在缺氧环境中将产生的NO2-N和剩余的NH3-N以及痕量的NO3-N转化为N2 (⑤式):
NH +1.5O →NO -+H O+H+ ④
NH +1.32NO -+H+→1.02N +0.26NO -+ 2H O ⑤
NH +0.85 O →0.11NO -+0.44N +0.14H++1.43H O
Anammox (Anaerobic ammonia oxidation,厌氧氨氧化) 是上世纪90年代发现的一种新型生物脱氮途径,由荷兰学者Mulder在一小型流化床反硝化反应器中首次发现. 早在1977 年,奥地利理论化学家Broda就曾预言自然界存在以硝酸盐或亚硝酸盐为氧化剂的厌氧氨氧化反应. 目前已确定的厌氧氨氧化菌有3种,即Brocadia [42]、Kuenenia [43]和Scaliadua [44, 45], 其中,Brocadia包括B. anammoxidans和B. fulgida,Kuenenia包括K. stuttgartiensis,Scalindua包括S. wagneri、S. brodae和S. sorokinii. 研究者将厌氧氨氧化的可能代谢途径归纳为图7.
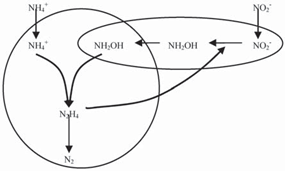
图7 厌氧氨氧化的可能代谢途径[16, 46]
Fig. 7 Hypothetical model of Anammox [16, 46]
厌氧氨氧化菌是专性厌氧菌,氧气会抑制其活性. Strous 等研究发现,限氧环境(空气饱和度<0.5%)对厌氧氨氧化菌的抑制是可逆的,被抑制后的厌氧氨氧化菌在厌氧状态下可恢复活性[47]. Schimidt等指出厌氧氨氧化菌与亚硝化单胞菌能共同生存于限氧环境中[48]. Jetten等通过FISH证实了在限氧条件下亚硝化菌能与厌氧氨氧化菌稳定共存[49]. 这些发现为单一反应器内实现半亚硝化–厌氧氨氧化工艺奠定理论基础.
通过15N示踪试验发现,厌氧氨氧化是以NO -而非NO -为电子受体[50]. 另有研究指出NO -也能用作厌氧氨氧化的电子受体[51],常规生物反硝化的两种中间产物NO -和N O也能用作厌氧氨氧化的电子受体[52].
厌氧氨氧化的主要产物为N2,有研究者发现N2O4也是终产物[53]. 其原因如本文第1部分所述,缺氧环境中硝化过程产物可能为N2O、NO、NO2 (N2O4)、N2,所以硝化–厌氧氨氧化反应体系会导致多种氮的气态产物产生.
4 总结与展望
4.1 关于污水生物脱氮系统中氮转化机制的研究对于污水处理过程非常重要,本文综述了好氧和限氧状态下氮素损失的微生物学机理,为非传统意义的总氮损失现象提供了生物学
方面的解释. 实际生物脱氮过程涉及多种微生物的协同、耦合作用,由于生物处理工艺的复杂性,一些反应过程的机理还不是很明确,需要进一步研究. 总结了目前已知的单级系统脱氮形式,如图8所示.
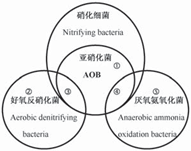
图8 单级好氧或限氧系统内的微生物脱氮形式
Fig. 8 Pattern of nitrogen removal in aerobic or oxygen-limited system
①自养亚硝化菌单独脱氮
①自养亚硝化菌单独脱氮(底物: NH3-N);② 好氧反硝化菌单独脱氮(底物: NH3-N);③自养(亚)硝化菌和好氧反硝化菌协同脱氮(底物: NH3-N);
④自养(亚)硝化菌和厌氧氨氧化菌协同脱氮(底物: NH3-N);⑤厌氧氨氧化(底物: NH3-N; NO2-N或NO3-N)
① Nitrogen removal by autotrophic nitrifying bacteria (Substrate: NH3-N);
② Nitrogen removal by aerobic denitrifying bacteria (Substrate: NH3-N);
③ Nitrogen removal by the cooperation of nitrifying bacteria and aerobic denitrifying bacteria (Substrate: NH3-N); ④ Nitrogen removal by the cooperation of nitrifying bacteria and Anammox bacteria (Substrate: NH3-N); ⑤ Anammox (Substrate: NH3-N; NO2-N or NO3-N)
4.2 基于传统理论的硝化–反硝化脱氮依然是自然界的主要脱氮途径,其脱氮贡献率要远远高于 “自养(亚)硝化菌脱氮”、“好氧反硝化脱氮”、“自养亚硝化菌和厌氧氨氧化菌的协同脱氮”这些脱氮新途径. 但是与传统的硝化–反硝化脱氮技术相比,这些新途径具有不可比拟的优越性,如可简化工艺,节省设备费用,降低氧气的供给,减少碱度消耗,减少甚至毋需碳源投加等等,因此关于这些脱氮新途径的研究对于强化污水生物脱氮具有重要意义.
4.3 近年来在这些新的脱氮途径研究的基础上产生了多种新型生物脱氮工艺,如:依据亚硝化菌的限氧氨氧化理论, 比利时Gent大学微生物生态实验室开发了OLAND (Oxygen limited autotrophic nitrification denitrfication)工艺;基于自养亚硝化菌和厌氧氨氧化菌的协同脱氮理论,2002年荷兰Delft工业大学首先提出新型生物脱氮工艺—— CANON (Completely autotrophic nitrogen removal over nitrite)工艺,以及厌氧氨氧化菌脱氮的ANAMMOX工艺和SHARON-ANAMMOX联合工艺. 如何将这些工艺大规模应用于工程实践,还有待进一步研究探索.
4.4 N O可以导致地球臭氧防护层的明显破坏,从而造成地球表层的不断升温,致温效应约为CO2的310倍,是一种重要的温室气体. 本文中提到的某些氮素去除途径中N2O可能作为硝化过程的副产物或者反硝化过程的产物而产生,所以在今后研究生物脱氮新途径时,也要加强对N2O产生条件及机理的研究,进而研究其减量化,避免N2O的产生.
4.5 分子生物学技术是研究生物反应机理的有效实验手段,可以为生化反应提供直接的证据. 近年来以FISH、PCR为代表的分子生物学技术已广泛应用于污水生物处理系统的微生物学研究,在环境微生物的多样性研究、特定微生物的原位分析以及微生物的功能研究方面取得了一定的成果. 迄今已有不少研究者将相关分子生物学技术应用于污水处理系统总氮损失的微生物学原理分析,可以预见,随着分子生物技术进一步的发展与应用,人们对水处理系统中生物反应机理的认识将会更加深入透彻.
References
1 Kraume M, Bracklow U, Vocks M, Drews A. Nutrients removal in MBRs for municipal wastewater treatment. Wat Sci Tech, 2005, 51 (6~7): 391~402
2 Helmer C, Kunst S. Simultaneous nitrification/denitrification in an aerobic biofilm system. Wat Sci Tech, 1998, 37 (4~5): 183~187
3 Kuai L, Verstraete W. Ammonium removal by the oxygen-limited autotrophic nitrification-denitrification system. Appl Environ Microbiol, 1998, 64: 4500~4506
4 Koch G, Siegrist H. Mathematical modeling of autotrophic denitrification in a nitrifying biofilm of a rotating biological contracter. Wat Sci Tech, 2000, 41: 191
5 Sun GZ, Austin D. Completely autotrophic nitrogen-removal over nitrite in lab-scale constructed wetlands: Evidence from a mass balance study. Chemosphere, 2007, 68 (6): 1120~1128
6 Bitchie GAF, Nicholas DJD. Identification of the sources of nitrogen oxide produced by oxiydative and reductive processes in N. europeae. Biochem J, 1972, 126: 1181~1191
7 Bock E, Wilderer PA, Freitag A. Growth of nitrobacter in the absence of dissolved oxygen. Water Res, 1988, 22 (2): 245~250
8 Bock E, Schmidt I, Stuven R, Zart D. Nitrogen loss caused by denitrifying Nitrosomonas eutropha cells using ammonium or hydrogen as electron donors and nitrite as electron acceptor. Arch Microbiol , 1995, 163: 16~20
9 Shrestha NK, Hadano S, Kamachi T, Okura I. Dinitrogen production from ammonia by Nitrosomonas europaea. Appl Catal A Gen, 2002, 237 (1): 33~39
10 Ahn Y. Sustainable nitrogen elimination biotechnologies: A review.Process Biochem, 2006, 41 (8): 1709~1721
11 Wrage N, Velthof GL, van Beusichem ML, Oenema O. Role of nitrifier denitrification in the production of nitrous oxide. Soil Biol Biochem, 2001, 33 (12~13): 1723~1732
12 Shrestha NK, Hadano S, Kamachi T, Okura I. Dinitrogen production from ammonia by Nitrosomonas europaea. Appl Catal A Gen, 2002, 237 (1~2): 33~39
13 Naqvi SWA, Noronha RJ. Nitrous oxide in the Arabian Sea. Deep Sea Res A Oceanogr Res Papers, 1991, 38 (7): 871~890
14 Wang JL (王建龙). 生物脱氮新工艺及其技术原理. China Water &Wastewater (中国给水排水), 2000, 16 (4): 25~28
15 Stuven R, Bock E. Nitrification and denitrification as source for NO and NO2 production in high-strength wastewater. Water Res, 2001, 35 (8): 1905~1914
16 Tallec G, Garnier J, Billen G, Gousailles M. Nitrous oxide emissions from denitrifying activated sludge of urban wastewater treatment plants,under anoxia and low oxygenation. Bioresour Technol, 2008, 99 (7): 2200~2209
17 Kampschreur MJ, van der Star WRL, Wielders HA, Mulder JW, Jetten MSM, van Loosdrecht MCM. Dynamics of nitric oxide and nitrous oxide emission during full-scale reject water treatment. Water Res, 2008, 3 (42): 812~826
18 Schmidt I, Hermelink C, van de Pas-Schoonen K, Strous M, den Camp HJO, Kuenen JG, Jetten MSM. Anaerobic ammonia oxidation in the presence of nitrogen oxides (NOx) by two different lithotrophs. Appl Environ Microbiol, 2002, 68 (11): 5351~5357
19 Zart D, Bock E. High rate of aerobic nitrification and denitrification by Nitrosomonas eutropha grown in a fermentor with complete biomass retention in the presence of gaseous NO2 or NO. Arch Microbiol, 1998,169: 282~286
20 Li XP ( 李小鹏). Study on the mechanisms of NO2 enhancing ammonium oxidation: [Master’s Degree Dissertation]. Chongqing, China (重庆): Chongqing University (重庆大学), 2004
21 Robertson LA, Kuenen JG. Aerobic denitrification: A controversy revived. Arch Microbiol, 1984, 139: 351~354
22 Patureau D, Zumstein E, Delgenes JP, Moletta R. Aerobic denitrification isolation from diverse natural and managed ecosystems. Microb Ecol, 2000, 39: 145~152
23 Kim YJ, Yoshizawa M, Takenaka S, Murakami S, Aoki K. Isolation and culture conditions of a Klebsiella pneumoniae strain that can utilize ammonium and nitrate ions simultaneously with controlled iron and molybdate ion concentrations. Biosci Biotechnol Biochem, 2002, 66 (5): 996~1001
24 Takaya N, Maria Antonina BCS, Yasushi S, Isao K, Zhou ZM, Hirofumi Sl. Aerobic denitrification bacteria that produce low levels of nitrous oxide. Appl Environ Microbiol, 2003, 69 (6): 3152~3157
25 Korner H, Zumft WG. Expression of denitrification enzymes in response to the dissolved oxygen level and respiratory substrate in continuous culture of Pseudomonas stutzeri. Appl Environ Microbiol, 1989, 55: 1670~1676
26 Lloyd D. Aerobic denitrification in soils and sediments: from fallacies to facts. Trends Ecol Evol, 1993, 8: 352~356
27 Wilson LP, Bouwer EJ. Biodegradation of aromatic compounds under mixed oxygen/ denitrifying conditions: A review. J Ind Microbiol Biotechnol, 1997, 18: 116~130
28 Joo HS, Hirai M, Shoda M. Characteristics of ammonium removal by heterotrophic nitrification-aerobic denitrification by Alcaligenes faecalis No. 4. J Biosci Bioeng, 2005, 100 (2): 184~191
29 Patureau D, Bernet N, Moletta R. Combined nitrification and denitrification in a single aerated reactor using the aerobic denitrifier Commonas sp. strain SGLY2. Water Res, 1997, 31 (6): 1363~1370
30 Gupta SK, Kshirsagar M. Quantitative estimation of Thiosphaera pantotropha from aerobic mixed culture. Water Res, 2000, 34 (15): 3765~3768
31 Bell LC, Ferguson SJ. Nitric and nitrous oxide reductase are active under aerobic conditions in cells of Thiosphaera pantotropha. J
32 Biochem, 1991, 273: 423~427 32 Wehrfritz JM, Reilly A, Spiro S, Richarson DJ. Purification of hydroxylamine oxidase from Thiosphaera pantotropha: Identifi cation of electron acceptors that couple heterotrophic nitrifi cation to aerobic denitrifi cation. FEBS Lett, 1993, 335: 246~250 33 Richardson DJ, Wehrfritz JM, Keech A, Crossman LC, Roldan MD, Sears HJ, Butler CS, Reilly A, Moir JWB, Berks BC, Ferguson SJ, Thomson AJ, Spiro S. The diversity of redox proteins involved in bacterial heterotrophic nitrifi cation and aerobic denitrifi cation. Biochem Soc Trans, 1998, 26 (3): 401~408 34 Joo HS, Hirai M, Shoda M. Improvement in ammonium removal efficiency in wastewater treatment by mixed culture of Alcaligenes faecalis No.4 and L1. J Biosci Bioeng, 2007, 103 (1): 66~73 35 He X (何霞), Lü J (吕剑), He YL (何义亮), Zhao B (赵彬), Li CJ (李 春杰). Study progress on the mechanism of heterotrophic nitrifi cation. Acta Microbiol Sin (微生物学报), 2006, 46 (5): 844~847 36 Hippen A, Rosenwinkel K, Baumgarten G, Seyfried CF. Aerobic deammonifi cation: A new experience in the treatment of wastewaters. Wat Sci Tech, 1997, 35 (10): 111~120 37 Third KA, Sliekers AO, Kuenen JG, Jetten MSM. The CANON system (Completely autotrophic nitrogen-removal over nitrite) under ammonium limitation: Interaction and competition between three groups of bacteria. Syst Appl Microbiol, 2001, 24 (4): 588~596 38 Gaul T, Filipov E, Schlosser N, Kunst S, Helmer-Madhok C. Balancing of nitrogen conversion in deammonifying biofi lms through batch tests and GC/MS. Wat Sci Tech, 2002, 46 (4, 5): 157~162 39 Pynaert K, Smets BF, Wyffels S, Beheydt D, Siciliano SD, Verstraete W. Characterization of an autotrophic nitrogen-removing biofi lm from a highly loaded lab-scale rotating biological contactor. Appl Environ Microbiol, 2003, 69: 3626~3635 40 Yu X, Qi ZH, Zhang XJ, Yu P, Liu B, Zhang LM, Fu L. Nitrogen loss and oxygen paradox in full-scale biofiltration for drinking water treatment. Water Res, 2007, 41 (7): 1455~1464 41 Kuenen JG, Jetten MSM. Extraordinary anaerobic ammonium-oxidizing bacteria. ASM News, 2001, 67 (9): 456~463 42 Kartal B, van Niftrik L, Sliekers O, Schmid MC, Schmidt I, van de PasSchoonen K, Cirpus I, van de Star W, van Loosdrecht M, Abma W, Kuenen JG, Mulder JW, Jetten MSM, den Camp HO, Strous M, van de Vossenberg J. Application eco-physiology and biodiversity of anaerobic ammonium-oxidizing bacteria. Rev Environ Sci Biotechnol, 2004, 3: 255~263 43 Egli K, Franger U, Alvarez PJJ, Siegrist H, van der Meer JR, Zehnder
33 AJB. Enrichment and characterization of ananmmox bacterium from a rotating biological contractor treating ammonium-rich leachate. Arch Microbiol, 2001, 175: 198~207 44 Kuypers MMM, Sliekers AO, Lavik G, Schmid M, Jorgensen BB, Kuenen JG, Sinninghe Damsté JS, Strous M, Jetten MSM. Anaerobic ammonium oxidation by anammox bacteria in the Black Sea. Nature, 2003, 422: 608~611 45 Schmid M, Walsh K, Webb R, Rijpstra WIC, van de Pas-Schoonen K, Verbruggen MJ. Candidatus “Scalindua brodae”, sp. nov., Candidatus “Scalindua wagneri”, sp. nov., two new species of anaerobic ammonium oxidizing bacteria. Syst Appl Microbiol, 2003, 26: 529~538
34 46 Van de Graaf AA, Mulder A, de Bruijn P, Jetten MS, Robertson LA, Kuenen JG. Anaerobic oxidation of ammonium is a biologically mediated process. Appl Environ Microbiol, 1995, 61: 1246~1251 47 Strous M, Heijnen JJ, Kuenen JG, Jetten MSM. The sequencing batch reactor as a powerful tool for the study of slowly growing anaerobic ammonium oxidizing microorganisms. Appl Microbiol Biotechnol, 1998, 50 (5): 589~596 48 Schmidt I, Sliekers O, Schmidt M, Cirpus I, Strous M. Aerobic and anaerobic ammonia oxidizing bacteria-competitors or natural partners. Microbiol Ecol, 2002, 39: 175~181 49 Jetten MSM, Sliekers O, Kuypers M, Dalsgaard T, van Niftrik L, Cirpus I, van de Pas-Schoonen K, Lavik G, Thamdrup B, Paslier De, Op den Camp HJM,
苏州湛清环保科技有限公司
热线:400-110-8500
传真:0512-50310052
邮箱:sales@drtsing.com
地址:江苏省苏州市昆山市玉山镇台虹路19号